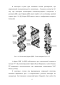Содержание к диссертации
Введение
ГЛАВА 1. Взаимодействие молекулы ДНК с комплексами платины и соединениями серебра 10
1.1 Структура молекулы ДНК 10
1.2 Комплексообразование ДНК с координационными соединениями металлов 10
1.2.1. Связывание молекулы ДНК с координационными соединениями платины - основа биологического действия противоопухолевых препаратов 15
1.2.2 Взаимодействие соединений серебра с молекулой ДНК в растворе 20
ГЛАВА 2. Методы исследования и материалы 25
2.1. Вискозиметрия 25
2.2. Динамическое двойное лучепреломление
2.3. Спектральные методы 27
2.4. Материалы 30
ГЛАВА 3. Исследование взаимодействия ДНК с соединениями платины и серебра 33
3.1. Сравнительный анализ комплексообразования ДНК с новыми биядерными соединениями платины и известным противоопухолевым препаратом цис-ДДП 33
3.2. Комплексы молекулы ДНК с соединениями серебра и металлизация полученных структур 88
Заключение 108
Список литературы 110
- Связывание молекулы ДНК с координационными соединениями платины - основа биологического действия противоопухолевых препаратов
- Взаимодействие соединений серебра с молекулой ДНК в растворе
- Динамическое двойное лучепреломление
- Комплексы молекулы ДНК с соединениями серебра и металлизация полученных структур
Связывание молекулы ДНК с координационными соединениями платины - основа биологического действия противоопухолевых препаратов
Открытие противоопухолевых свойств цис-дихлордиамминплатины (II) (цис-ДДП, цисплатина) произошло случайно. С 70-х гг. прошлого века исследование взаимодействия ДНК с соединениями платины проводится очень активно [9-17]. Интрига заключалась в том, что изменение расположения лигандов в координационной сфере платины приводила к потере противоопухолевой активности соединения (см. на рис. 1.6 структуру активного препарата цис-ДДП и его неактивного транс-изомера). Цисплатин активно применяется при лечении опухолей мочевого пузыря, шеи, головы, а также мелкоклеточного рака легких через внутривенное введение [11].
Процесс попадания препаратов платины в клетки изучен достаточно хорошо [15,18]. ДНК является главной мишенью для цисплатина [19, 20]. По одному атому платины приходится на 3 104—3 105 молекул белка и 10-1000 молекул РНК. Каждая молекула ДНК связывает около 9 атомов платины, однако именно такое связывание имеет биологический эффект. Цис-ДДП блокирует репликацию ДНК [21-24] через образование координационной связи с основаниями (преимущественно гуанином). При этом наблюдается ярко выраженная избирательность к GC-парам [25, 26]. При комплексообразовании происходит последовательное замещения хлора в координационной сфере платины на воду (что приводит к образованию акваформы [Pt(NH3)2(H20)Cl]+ или [Pt(NH3)2(H20)2]2+), а затем вода замещается на N7 атом гуанина или аденина. Причем присоединение к аденину было обнаружено только на второй стадии связывания цис-ДДП с ДНК, то есть после того, как один из атомов хлора заместился на N7 атом гуанина [27].
При взаимодействии с ДНК аквапроизводных цис-ДДП сначала образуется одна координационная связь (монофункциональный аддукт), а затем вторая (бифункциональный аддукт) (рис. 1.7). Для реализации такого взаимодействия необходимо время не менее 4 часов при 37С [28 - 32].
Бифункциональные аддукты могут быть с образованием как межнитевых, так и внутринитевых сшивок, возможны также монофункциональные аддукты (рис. 1.8) [33-36].
В отличие от цис-ДДП, транс-ДДП формирует, в основном, монофункциональные аддукты ( 50 %), хотя образуется и некоторое количество 1,1 межнитевых сшивок (-12 % для линейной ДНК) предпочтительно между гуанином и комплементарным цитозином [37, 38].
При образовании большого количества комплексов цис-ДДП с ДНК наблюдается уменьшение стабильности спирали [40,41], тогда как малое количество аддуктов (при г 0,4, где г — отношение количества атомов платины к числу пар оснований ДНК) не вызывает дестабилизации двойной спирали [42]. Изменение рН в растворах, содержащих комплексы ДНК с препаратами платины, не приводит к протонированию ДНК, наблюдаемому обычно при определённых значениях рН, что свидетельствует о блокировании платиной основного протон-акцепторного центра двуспиральной ДНК (N7 гуанина) [43]. 1,2-внутринитевые сшивки d(GpG) могут являться главной причиной изгиба спирали ДНК, - она изгибается примерно на 60 по направлению к большой бороздке [44,45].
Несмотря на достаточно успешное использование цис-ДДП в качестве противоопухолевого препарата, ее отрицательные качества (плохая растворимость в воде, высокая токсичность и неизбирательность действия) требуют поиска эффективных заменителей этого лекарственного средства и стимулируют интерес к синтезу и изучению биологической активности новых соединений, не обладающих такими отрицательными характеристиками. В этой связи синтез и изучение альтернативных соединений платины с различными лигандами в первой координационной сфере платины является перспективным направлением.
Одним из направлений синтеза новых препаратов является синтез двуядерных соединений, содержащих два атома платины. В частности, перспективным является синтез соединений платины триаминового типа [46,47]. Моноядерный триамин платины [Р1:(Мїз)зС1]С1 не обладает противоопухолевой активностью. Введение более крупного амина в качестве лиганда в цис-положение к атому хлора может представлять интерес для проверки на цитотоксичность. Биядерные комплексы платины триаминового типа с цис-расположением аминовых лигандов проявляли большую активность по сравнению с аналогичными моноядерными комплексами [48].
Ранее в лаборатории молекулярной биофизики изучали взаимодействие молекулы ДНК в растворе с биядерным соединением двухвалентной платины [Pt(NH3)2Cl-R-Cl (NH3)2Pt]Cl2, где R - пиразин [49]. Было показано, что такой препарат связывается с ДНК, формируя бидентатный комплекс (по одной координационной связи у каждого атома платины), провоцирующий существенный изгиб спирали в месте образования комплекса. Использование биядерных комплексов платины триаминового типа может не только увеличить эффективность действия препаратов, но и облегчить их использование на практике, так как в отличие от плохо растворимой в воде цис-ДДП они являются электролитами.
Следует отметить большой интерес к комплексам платины с азотосодержащими гетероциклами (рис. 1.9), которые могут повышать активность цис и транс соединений платины [50-53]. Наибольший интерес привлекают соединения с пиридином или его производными [54-63].
В работе [66] показано, что соединения платины биядерного типа с тетразольным лигандом активнее триазолатных и пиразолатных аналогов. Исследовались также соединения trans- [ML2Cl2](M=Pt, Pd) и cis-[PtL2Cl2], где L - 1- или 2-замещенный 5-аминотетразол [67] и тетразолосодержащие препараты [68, 69] - описаны синтез производных тетразоло [1,5-а] хинолина, их биологическая активность, и цитотоксичность комплексов двухвалентной платины с такими лигандами.
Изучение молекулярного механизма связывания новых соединений с молекулой ДНК в растворе может служить предварительным тестом на их биологическую активность. В задачу работы входило изучение конформационных изменений ДНК при ее взаимодействии с рядом соединений платины, сравнение молекулярного механизма действия новых препаратов с результатом связывания цис-ДДП с молекулой ДНК.
Взаимодействие соединений серебра с молекулой ДНК в растворе Как известно, структура любого координационного соединения металла включает в себя ион-комплексообразователь (платина, железо, кобальт, рутений и др.), лиганды внутренней координационной сферы, не диссоциирующие при растворении вещества в воде, и так называемые внешнесферные лиганды, диссоциирующие с образованием комплексного иона и его противоионов в растворе [16] (рис. 1.10). Количество потенциальных мест связывания лигандов во внутренней координационной сфере иона называют координационным числом.
Взаимодействие соединений серебра с молекулой ДНК в растворе
При измерении вязкости растворов основным параметром является их относительная вязкость цг = ц/щ ( где ц — вязкость раствора, rj0 — вязкость растворителя). Вязкость растворов полимеров зависит от градиента скорости потока, поэтому принято проводить измерения относительной вязкости при разных g с последующей экстраполяцией к g=0. При использовании низкоградиентного ротационного вискозиметра оригинальной конструкции типа Зимма-Крозерса [89 - 91] градиенты находятся в диапазоне до 5 с"1. В работе измерение величины цг проводили при разных градиентах скорости потока g в диапазоне от 0,5 до 1,5 сек"1. Для всех растворов, исследуемых в работе, градиентная зависимость в используемом диапазоне значений g отсутствовала. Для определения значения величины цг при нулевом градиенте скорости полученные при разных g величины усредняли. Величину удельной вязкости Цуд = (ц - Цо)/щ = (цг- 1) использовали для вычисления величины приведенной вязкости растворов Yjnp = (rjr -1)/С, где С - концентрация раствора. Для определения значения характеристической вязкости ДНК в растворе [ц] строили зависимость цпр от концентрации ДНК С. Для описания этой зависимости используется степенной ряд:
Это так называемая экстраполяция по Хаггинсу, где к1у к2 — константы Хаггинса. Обычно ограничиваются областью линейной зависимости (rjr-l)/C от С. Полученную концентрационную зависимость экстраполировали
Величина [ц] пропорциональна удельному объему полимерного клубка в растворе. Для макромолекул достаточно большой молекулярной массы, имеющих конформацию статистического клубка в растворе, справедлива формула Флори: где h2 12 — среднеквадратичное расстояние между концами полимерной цепи в реальном растворе, которое характеризует линейный размер молекулярного клубка, М — молекулярная масса полимера, Ф — параметр Флори, в общем случае зависящий от объемных эффектов и жесткости полимера, а — коэффициент линейного набухания макромолекулы, а = h2 1/2/ h02 1/2 , где ho m - среднеквадратичное расстояние между концами невозмущенной (гауссовой) цепи, для которой справедливо: h0 = LA, где L — гидродинамическая длина макромолекулы, А — длина статистического сегмента в Куновской модели полимерной цепи (параметр, характеризующий изгибную жесткость цепи). Для высокомолекулярной ДНК А = 2а, где а — персистентная длина.
Зависимость величины двойного лучепреломления An растворов ДНК от градиента скорости потока g определяли на установке с полутеневым эллиптическим компенсатором. Величину (An/g)0 и величину относительной вязкости того же раствора г\г, определенные при g 0, использовали для вычисления величины приведенного двойного лучепреломления (An/g)(/(rjr-l)rj0, которое для растворов ДНК не зависит от ее концентрации и совпадает с отношением [п]/[ц] (где [п] — динамооптическая постоянная, [п] = limc offdn/gJg t/Crjo]. В этом случае можно пренебречь возможным вкладом эффекта формы. Для высокомолекулярной ДНК справедливо [92, 93]: температура, к — постоянная Больцмана, Aa=ai-a2 — разность главных поляризуемостей статистического сегмента макромолекулы в приближении его цилиндрической формы. Таким образом, измеряя в эксперименте величину An/g(r\-r\o) для растворов ДНК различных концентраций, можно определить значение Аа, связанное с жесткостью макромолекулы, выраженной через число мономерных остатков S (нуклеотидных пар) в статистическом сегменте: A a = SAfi. Здесь Afi - разность поляризуемостей пары нуклеотидов вдоль оси спирали ДНК и перпендикулярно ей.
Изучение спектральных свойств ДНК при ее взаимодействии с биологически активными соединениями может дать информацию как о состоянии вторичной структуры макромолекулы, так и о возможных изменениях электронной структуры соединений в процессе комплексообразования. Спектр поглощения молекулы ДНК имеет выраженную полосу лг-л: и п-7г переходов азотистых оснований с максимумом 260 нм, интенсивность которой возрастает при денатурации ДНК (гиперхромный эффект). В области длин волн более 300 нм ДНК не поглощает. Спектры поглощения ДНК и ее комплексов с различными соединениями регистрировали на спектрофотометре СФ-56 (Россия). Концентрацию ДНК определяли по разнице оптической плотности гидролизованных с 6 % НСЮ4 растворов при X = 270 нм и X = 290 нм. Величину є2во(р) вычисляли по формуле:
Круговой дихроизм, обусловленный различным поглощением лево- и право- поляризованного света в растворах оптически активных веществ, отражает хиральность одного или нескольких компонентов изучаемых систем. Величина кругового дихроизма, представляемая в виде разницы коэффициентов молярной экстинкции при поглощении лево- и право поляризованного света Ає=Єі-єг, связана с молярной эллиптичностью [в], соотношением [0]= ЗЗООАє. Спектры кругового дихроизма регистрируются в тех спектральных областях, где образец поглощает свет, при этом величина Ає (или [в]) может быть как положительной, так и отрицательной. Знак и интегральная интенсивность полос КД зависят от структуры молекулы и ее комплексов. Изучение оптической активности может быть использовано для выявления конформационных изменений молекул при взаимодействии и влияния локального окружения хромофоров, так как метод отличается высокой чувствительностью к таким изменениям. Изменение спектров КД отражает, в основном, изменения локальной структуры в системе, если таковые происходят.
Динамическое двойное лучепреломление
Для выявления особенностей комплексообразования биядерных соединений платины с ДНК мы приводим результат изучения спектров поглощения ДНК при ее связывании с цис-ДДП. Как известно, основной моделью для такого комплексообразования является связывание препарата с соседними гуаниновыми основаниями одной цепи. Вместе с тем, один из описанных ранее комплексов, когда платина образует координационную связь с основаниями разных цепей ДНК, лучше объясняет противоопухолевое действие цис-ДДП, открытие которого было основано на наблюдаемом Розенбергом филаментном росте E.coli в присутствии цисплатина [9,10]. Естественно предположить, что в процессе связывания цис-ДДП с молекулой ДНК реализуются разные комплексы [42, 99, 100].
Для комплексов ДНК с цисплатином наблюдается характерное изменение спектра поглощения ДНК, фиксируемое обычно при связывании различных препаратов с атомом N7 гуанина [99]: это небольшой батохромный сдвиг полосы и гипохромный эффект при малых концентрациях соединений, который сменяется гиперхромным эффектом, проявляющимся при их больших концентрациях. Гиперхромизм является результатом дестабилизации вторичной структуры ДНК вследствие ослабления водородных связей из-за перераспределения заряда в гетероциклах оснований и нарушения стэкинга после атаки ионами (или лигандами) N7 гуанина. Бидентатный комплекс цис-ДДП с соседними пуриновыми основаниями одной цепи (1,2 intrastrand crosslink) сопровождается характерным изменением спектров КД ДНК [99,100]. Увеличение амплитуды и батохромний сдвиг положительного максимума с ростом концентрации цисплатина трансформируется в уменьшение интенсивности положительной полосы спектра КД ДНК и сдвиг нуля (для соединений Pt-1, Pt-2, Pt-З не наблюдается такого изменения в спектре КД ДНК, которое бы свидетельствовало об образовании бидентатного комплекса). Концентрации, при которых происходит качественное изменение спектров КД, согласуются с концентрациями, при которых наблюдаются описанные выше изменения спектра УФ поглощения ДНК. Такое поведение спектральных параметров указывает на преимущественное формирование разных комплексов в зависимости от концентрации цисплатина в растворе. При малых C(Pt) проявляется влияние бидентатного комплекса, затем в результате дестабилизации вторичной структуры ДНК в месте связывания платины открываются новые потенциальные центры связывания на противоположной цепи ДНК, в том числе занятые ранее в формировании водородных связей. При этом возможно формирование координационных связей, обеспечивающих существование 1,1 interstrand crosslinks или 1,2 interstrand crosslinks, которые стабилизируют комплекс. Как уже отмечалось, обычно одновременно в растворе ДНК с цисплатином реализуются различные типы комплексов с преобладанием того или иного в зависимости от концентраций взаимодействующих агентов и состояния вторичной структуры ДНК. В том числе, кроме описанных выше, происходит взаимодействие акватированной формы цисплатина с фосфатами ДНК, реализуется монодентатное связывание платины с гетероциклическими атомами азота оснований и др.
Отметим, что при рассмотрении спектров КД ДНК в присутствии изучаемых соединений платины Pt-2 и Pt-З (соединения не проявляют оптической активности) можно видеть лишь изменения второго типа, которые одинаковы для обоих соединений (рис. 3.1.14), - уменьшение амплитуды положительной полосы. И в спектре УФ поглощения можно видеть сходство в действии препаратов Pt-2 (как и Pt-З) и цис-ДДП. Они наблюдаются примерно при сходных концентрациях соединений в растворе ДНК. На основании этого можно заключить, что в связывании с ДНК участвует лишь один атом платины соединений Pt-2 и Pt-З. Таким образом, при отсутствии комплекса первого типа (бидентатного комплекса платины с соседними основаниями ДНК) при связывании Pt-2 и Pt-З с ДНК возможно формирование иных комплексов, характерных и для цис-ДДП.
Ранее в лаборатории подробно изучали взаимодействие с ДНК биядерного соединения Pt-4 в 0,005 М и 1 М NaCl [49], которое имеет сходное строение с соединениями Pt-З и Pt-2, но в качестве общего для двух атомов платины лиганда выступает не пятичленное гетероциклическое соединение тетразол (метилтетразол), а шестичленный гетероцикл пиразин. Выбор используемых в экспериментах концентраций соли (0,005 М и 1 М NaCl) позволяет выделить электростатическую составляющую взаимодействия, так как в 1 М NaCl полиэлектролитное набухание ДНК подавлено, а отрицательно заряженные фосфатные группы достаточно эффективно экранированы противоионами. В 0,005М NaCl, напротив, электростатические взаимодействия проявляются ярко, но при этом не происходит еще изменения персистентной длины ДНК из-за ближних электростатических взаимодействий [93]. Проведенное в работе сопоставление действия новых соединений Pt-2, Pt-З, Pt-1 с Pt-4 позволило сделать дополнительные заключения о взаимодействии платиновых соединений с ДНК.
Так как соединения представляют собой электролитные комплексы, в отличие от цис- и транс-ДДП, они хорошо растворимы в воде, и после диссоциации хлора приобретают положительный заряд +2 (соединение Pt-1) или +1 (соединения Pt-2 и Pt-З). Положительный заряд соединений в растворе способствует их электростатическому притяжению к отрицательно заряженной молекуле ДНК. В результате реакции акватации (не протекающей для Pt-І) соединения Pt-2 и Pt-З приобретают дополнительный положительный заряд, который может доходить до +3. Это обеспечивает сильное электростатическое взаимодействие соединений с отрицательно заряженной ДНК. Обычно при исследовании растворов ДНК используют низкомолекулярный поддерживающий электролит (NaCl). Вариация концентрации соли позволяет моделировать ионную силу венозной крови и внутриклеточной жидкости.
Известно, что цис- и транс-ДДП не взаимодействуют с ДНК в 1 М NaCl [99, 100]. Аналогично, для Pt-1, Pt-2 и Pt-З мы не наблюдаем взаимодействия с макромолекулой при больших концентрациях соли, хотя оно ярко проявляется в растворах малой ионной силы (0,005 М NaCl). Это указывает на важную роль электростатических взаимодействий при комплексообразовании. Дальнодействующие электростатические взаимодействия способствуют сближению соединений платины и ДНК, после чего происходит образование комплекса, который дополнительно может быть стабилизирован с помощью Ван-Дер-Ваальсовых сил и водородных связей.
Эксперимент показал [49], что соединение Pt-4 образует комплексы с молекулой ДНК даже в растворах большой ионной силы (1 М NaCl). В отличие от Pt-2 Pt-З, заряд этого соединения после растворения в воде равен +2. В результате акватации он может достигать значения 4+. Ранее в лаборатории изучали взаимодействие молекулы ДНК с двухвалентными ионами металлов [98, 99]. Было показано, что при заряде +2 ионы взаимодействуют с молекулой ДНК даже при значительной концентрации одновалентных противоионов в растворе (в 1 М NaCl), хотя при этом они не вызывают уменьшения объема макромолекулы, так как полиэлектролитное набухание в этих условиях подавлено. По-видимому, в случае Pt-4 не только заряд соединения в растворе является причиной образования комплекса с ДНК в 1 М NaCl.
Комплексы молекулы ДНК с соединениями серебра и металлизация полученных структур
Результаты, изложенные в этом разделе, полностью опубликованы в работе [75]. Металлическое серебро традиционно считается бактерицидным. Переход к наноразмерным объектам может значительно изменить свойства веществ. В последнее время в медицинских целях интенсивно проводятся исследования биологической активности наночастиц серебра [109, ПО]. Их сопряжение с биополимерами в качестве носителя интересно не только в целях развития молекулярной медицины, но и для новых разработок в области наноэлектроники и нанооптики [111, 112].
Наночастицы серебра интересны своими уникальными оптическими свойствами: их коллоидные растворы имеют специфическую полосу поглощения в видимой области спектра, обусловленную плазмонным резонансом. Изменение этой полосы под действием различных факторов дает возможность следить за состоянием наночастиц и их окружения в растворе. Наночастицы металлов можно использовать для обнаружения, визуализации и лечения злокачественных опухолей. В связи с этим изучение взаимодействия наночастиц металлов с молекулой ДНК в растворе интересно с разных точек зрения.
Кроме сопряжения макромолекул с уже готовыми наночастицами перспективным приемом является металлизация молекулы ДНК в растворе после образования ее комплексов с ионами серебра. Для этого используют различные восстановители, в частности, боргидрид натрия. Подробное изучение влияния компонентов взаимодействия на состояние молекулы ДНК в растворе даст основания для направленной металлизации макромолекулы в растворе при решении различных задач. Например, такой подход используется при создании нанопроволок [113]. Для металлизации ДНК необходимо предварительное связывание с молекулой ДНК соединений серебра [114, 115], которые в дальнейшем послужат точками роста восстановленного серебра на макромолекуле.
В настоящей работе проводится сравнение роли ионов серебра и координационного соединения серебра с фенантролиновыми лигандами в процессе связывания с макромолекулой и дальнейшей металлизации ДНК.
При работе с соединениями серебра ДНК растворяли в дистиллированной воде, и после 5 дней хранения при температуре 4 С в раствор добавляли NaN03 (а не NaCl как обычно) для достижения требуемой ионной силы (обычно 0,005 М). Растворы ДНК центрифугировали или фильтровали перед использованием. В качестве компонентов для синтеза наночастиц (соединение серебра и восстановитель) использовали коммерческие препараты: серебро азотнокислое AgN03, боргидрид натрия NaBH4 и соединение серебра, условно обозначаемое как Ag-Phen (рис.3.2.1). Боргидрид натрия растворяли в дистиллированной воде непосредственно перед употреблением. Соединение Ag-Phen в водном растворе диссоциирует с образованием комплексного иона с зарядом +1.
На первом этапе исследований после смешивания раствора ДНК в 0,005 М NaN03 с раствором AgN03 образование комплекса ионов серебра с молекулой ДНК контролировали по характерным изменением спектров УФ поглощения ДНК (рис. 3.2.2) и кругового дихроизма (КД) макромолекулы (рис. 3.2.3). В спектре УФ поглощения ДНК наблюдается смещение максимума, появление плеча и небольшой гипохромный эффект, который с увеличением концентрации серебра в растворе трансформируется в гиперхромный. Наблюдаемые изменения в спектре поглощения ДНК обычно приписывают связыванию ионов металлов с молекулой ДНК по позиции N7 гуанина [98, 99]. Действительно, присоединение серебра приводит к изменению распределения электронной плотности в гетероциклическом основании, что сопровождается соответствующими спектральными изменениями. Такое связывание приводит к дестабилизации водородных связей между комплементарныими парами, а при значительном количестве таких сайтов связывания наблюдается нарушение стэкинга оснований, сопровождающееся гиперхромным эффектом в спектре поглощения ДНК.
Спектры поглощения ДНК в комплексе с ионами серебра (а) и результат анализа этих спектров (б) - зависимость оптической плотности растворов при двух длинах волн 260 нм (1) и 275 нм (2) от концентрации серебра в растворе. C(DNA) = 0.0025%. Через сутки после приготовления систем (при хранении растворов при температуре 4 С ) спектры не изменились, что свидетельствует о стабильности комплексов. Спектры КД ДНК при добавлении в раствор нитрата серебра изменяются существенно. Это сложно объяснить одним связыванием ионов серебра с азотистыми основаниями ДНК, так как ионы переходных металлов при связывании с азотистыми основаниями макромолекулы вызывают существенно меньшее изменение спектра КД ДНК, а ионы щелочноземельных металлов практически не меняют форму спектра, индуцируя лишь уменьшение интенсивности положительной полосы [98, 99].
Спектры кругового дихроизма ДНК в комплексе с Ag+ (при использовании нитрата серебра) в 0,005 М NaN03 при разных С (Ag), концентрации приведены на рисунке.
Наблюдаемую на опыте сильную трансформацию спектра КД ДНК, который кардинально отличается от спектров КД ДНК в растворах одно-двух- и трехвалентных ионов металлов, объяснить достаточно сложно.
Возможно, при связывании происходит частичное восстановление серебра [75], что может вызвать появление рассеяния в растворе, сложным образом влияющее на вид спектра КД ДНК.
На рисунке 3.2.4 приведены спектры поглощения растворов, содержащих компоненты взаимодействия, необходимые для формирования наночастиц, при разной очередности их добавления. После добавления ДНК в раствор, где произошло восстановление серебра (раствор содержал сформированные наночастицы, спектр 3) плазмонный пик смещен в коротковолновую область относительно наблюдаемого для системы, когда восстановление серебра происходило после образования комплексов макромолекулы с ионами серебра (к раствору ДНК последовательно добавляли AgN03 и NaBH4). В последнем случае через минуту после добавления восстановителя интенсивность пика мала (спектр 2), но через 75 минут она становится равной наблюдаемой для предыдущей системы (см. спектр 4). Анализ показывает, что спектр поглощения ДНК не зависит от порядка добавления нитрата серебра и боргидрида натрия в раствор (полоса с максимумом 260 нм). Вместе с тем, полоса плазмонного резонанса при добавлении ДНК в раствор с наночастицами появляется сразу, она более ярко выражена и не меняется через 75 минут, в отличие от соответствующей полосы в спектре 2. Вместе с тем, сравнивая полученные данные со спектром поглощения коллоидного раствора серебра без ДНК (спектр 6), можно отметить длинноволновой сдвиг соответствующей полосы в присутствии ДНК. Когда через 75 минут полосы плазмонного резонанса для систем с ДНК сравниваются по интенсивности, для ионов серебра, предварительно связанных с ДНК, восстановление в течение 75 минут приводит к небольшому длинноволновому сдвигу максимума. Можно предположить, что сразу после добавления в раствор ДНК с AgN03 боргидрида натрия происходит восстановление не связанных с ДНК ионов серебра. Действительно, тимусная ДНК содержит около 45% ГЦ пар, то есть при полном заполнении возможных сайтов связывания в большой бороздке ДНК достаточно много ионов серебра остаются в растворе и могут формировать наночатицы сразу после добавления восстановителя. Полагаем, что только такие частицы вносят вклад в полосу плазмонного резонанса, зафиксированную сразу после добавления восстановителя (спектр 2), тем более, что положение максимума этой полосы совпадает с наблюдаемым в спектре 3. Вычитая спектр 2 из спектра 4, получим полосу плазмонного резонанса для наночастиц, восстановленных непосредственно на ДНК (для частиц, которые формируются через 75 минут после добавления восстановителя, спектр 5). Нормализованные на максимум плазмонной полосы спектры показывают, что, действительно, существуют две спектральные формы наночастиц в растворе ДНК, отражающие наличие наночастиц, сформированных при восстановлении свободных ионов в растворе и при восстановлении ионов на ДНК (более длинноволновой максимум). Вместе с тем, присутствие ДНК все же оказывает влияние на состояние свободных наночастиц, так как без нее плазмонная полоса в спектре 6 сдвинута в коротковолновую область.
Спектры поглощения растворов ДНК (а) в 5 mM NaN03 (1), через минуту после последовательного добавления нитрата серебра и боргидрида натрия (2), после добавления в раствор ДНК предварительно смешанных растворов AgN03 и NaBH4 (3), а также раствор (2) через 75 минут (4), вычисленный пик плазмонного резонанса для наночастиц, восстановленных на ДНК (5), полученный вычитанием спектра (2) из спектра (4), и полоса плазмонного резонанса для наночастиц, полученных без добавления ДНК (6). С(ДНК)=0,008% =2,4х10 4М (bp), C(AgN03) = 2,7х10"4М, C(NaBH4) = 2,2х10 3М. Справа ( б ) приведены те же спектры, нормализованные на максимум плазмонного пика.