Содержание к диссертации
Введение
Глава 1. Обзор литературы: р2-рецепторы в кровеносных сосудах человека 13
1.1. Современные представления о роли Р2-рецепторов в регуляции тонуса кровеносных сосудов 14
1.2. Наличие и функциональная роль Р2-рецепторов в кровеносных сосудах человека 20
1.3. Нейрональный контроль тонуса большой подкожной вены бедра человека 23
1.4. Альтернативные артериальные кондуиты для шунтирующих операций на сердце и возможные механизмы их спазмирования 27
1.5. Р2-рецепторы кровеносных сосудов как перспективные мишени воздействия новых лекарственных препаратов 29
Глава 2. Материалы и методы исследований 33
2.1. Характеристика пациентов и метод интраоперационного забора
материала для исследований 33
2.2. Исследование механической активности изолированных кровеносных сосудов человека 39
2.3. Иммуногистохимические методы исследования 50
2.4. Анализ результатов исследований 56
2.5. Использованные вещества 57
2.6. Этические вопросы 58
Глава 3. Результаты собственных исследований 59
3.1. Влияние норэпинефрина, гистамина и агонистов и антагониста Р2 рецепторов на механическую активность артерии желчного пузыря человека з
3.2. Влияние норэпинефрина, гистамина и агонистов Р2-рецепторов на механическую активность желудочно-сальниковой артерии человека 65
3.3. Влияние норэпинефрина, гистамина и агонистов Р2-рецепторов на механическую активность лучевой артерии 69
3.4. Влияние норэпинефрина, гистамина и агонистов Р2-рецепторов на тонус и сократительную активность варикозно-измененной большой подкожной вены человека на разных уровнях 73
3.5. Сравнение влияния агониста Р2-рецепторов ,-метилен-АТФ и
антагониста Р2-рецепторов PPADS на варикозно-измененной и не
пораженной варикозной болезнью большой подкожной вене человека 76
3.6 Зависимость сократительной способности варикозно-измененной большой подкожной вены от протяженности рефлюкса и класса хронических заболеваний вен 78
3.7 Влияние электрической стимуляции неадренергических, нехолинергических нервов на тонус и сократительную активность большой подкожной вены человека на разных уровнях 83
3.8 Иммуногистохимическое исследование наличия и локализации подтипов Р2-рецепторов в артерии желчного пузыря 87
Глава 4. Обсуждение 91
Заключение 101
Выводы 103
Практические рекомендации 105
Список сокращений 106
Список литературы
- Нейрональный контроль тонуса большой подкожной вены бедра человека
- Исследование механической активности изолированных кровеносных сосудов человека
- Влияние норэпинефрина, гистамина и агонистов Р2-рецепторов на механическую активность лучевой артерии
- Зависимость сократительной способности варикозно-измененной большой подкожной вены от протяженности рефлюкса и класса хронических заболеваний вен
Введение к работе
Актуальность исследования
В последние несколько десятилетий Р2-рецепторы, основным эндогенным
лигандом которых вляется аденозин-трифосфорная кислота (АТФ), были
обнаружены во многих кровеносных сосудах человека и животных (Зиганшин А.У.,
Зиганшина Л.Е. 2009; Burnstock G., 2014). Р2-рецепторы делятся на 2 больших
семейства - Р2Х и Р2Y, которые отличаются своей структурой, функцией и
механизмом реализации эффекта. РХ-рецепторы - это типичные иганд-
оперирующие ионные каналы, в о врмя кк Р2У-рецепторы по мханиму
активации являются метаботропными G-протеин опосредованными рецепторами
(Burnstock G., 2007). Локализующиеся на поверхности гладко мышечных клеток
Р2Х-рецепторы в основном опосредуют тонизирующее действие агонистов этих
рецепторов на сосуды, тогда как находящиеся на эндотелии Р2У-рецепторы, за
некоторыми исключениями, обеспечивают вазодилятацию (Burnstock G., 2009). В
последние годы накапливаются исследования, направленные на изучение роли
внеклеточной АТФ сердечно-сосудистой системе человека в целом и в
кровеносных сосудах, в частности (Burnstock G. et al., 2014). Последние обзорные работы свидетельствуют о реальной потенциальной возможности использования агонистов и антагонистов Р2-рецепторов в клинической практике (Burnstock G. et al., 2014, Ralevic V., 2015, Ralevic V. et al., 2015).
Известно, что поверхностная венозная система, в частности, большая подкожная вена (БПВ) бедра, более других подвержена изменениям при варикозной болезни. Осложнения варикозной болезни вен в виде дерматитов, целлюлитов, кровотечений, тромбофлебитов и трофических язв часто приводят к длительной утрате трудоспособности, иногда являясь причиной инвалидности (Бураковский В.И. и др., 1996; Gloviczki P. et al., 2011). Однако этиология и патогенез варикозного поражения вен нижних конечностей о настоящего времени полностью не раскрыты. Поэтому оправданным может быть применение при этом заболевании эффективных вазотонических средств, которыми в перспективе могли бы явиться агонисты Р2-рецепторов.
Существуют предположения, что варикозная болезнь поражает не весь ствол большой подкожной вены, а лишь некоторые ее участки (Golledge J. et al., 2003). Это имеет важное значение в клинической практике, поскольку большая подкожная вена является удобным и наиболее асто используемым аутотрансплантатом при различных шунтирующих операциях (аортокоронарное шунтирование, бедренно-подколенное шунтирование, и т.д.). В связи с этим, уточнение конкретных участков поражения большой подкожной вены является важным для определения тактики хирургического лечения и объема оперативного вмешательства при варикозной болезни с целью проведения вено-сохраняющих вмешательств.
Современным часто использующимся методом лечения ишемической болезни сердца является аортокоронарное шунтирование, основанное на формировании новых сосудистых бассейнов (Serruys P.W. et al., 2009). В качестве аутотрансплантата при этой операции чаще всего используют большую подкожную вену, а также некоторые артериальные сосуды - внутреннюю грудную, лучевую и желудочно-сальниковую артерии. Основной проблемой при операциях по реваскуляризации миокарда являются осложнения в послеоперационном периоде, связанные с вазоспазмом и тромбозом шунтов (в частности, большой подкожной
4 вены, лучевой артерии и желудочно-сальниковой артерии), что нередко является причиной летальности (Uydes-Dogan B.S. et al., 1996; Ding R. et al., 2008; Ustunsoy H. et al., 2009; Sarandria D. et al., 2011; Rehman S.M. et al., 2013). Поэтому актуально изучение механизмов вазоконстрикции большой подкожной вены, лучевой артерии, желудочно-сальниковой артерии и поиск эффективных способов ее профилактики, возможно, посредством воздействия на Р2-рецепторы.
Все вышесказанное подчеркивает важность и актуальность изучения наличия и функциональной активности Р2-рецепторов в кровеносных сосудах человека. Ранее в нашей лаборатории было показано наличие Р2-рецептор-опосредованных ответов в некоторых кровеносных сосудах, используемых как аутотрансплантаты при аортокоронарном шунтировании (Хазиахметов Д.Ф., 2003) и в ушке правого предсердия человека (Рычков А.В., 2007). Настоящее исследование является продолжением этих работ в отношении исследования других кровеносных сосудов (артерия желчного пузыря, желудочно-сальниковая артерия, лучевая артерия), а также выявления новых Р2-рецептор-опосредованных эффектов а анее исследованных сосудах (большая подкожная вена).
Цель исследования
Изучить особенности отвтов различных кровеносных осудов чловка,
вызванных агонистами -рецепторов, овести сравнительную
фармакологическую характеристику.
Задачи исследования
-
Провести сравнительную фармакологическую характеристику механической активности артерии желчного пузыря, желудочно-сальниковой артерии и лучевой артерии человека, вызванных агонистами Р2-рецепторов - АТФ, ,-метилен-АТФ, УТФ, 2-метилтио-АТФ, а также норэпинефрином гистамином;
-
Установить особенности Р2-рецептор-опосредованных тветов большой подкожной вены у пациентов с варикозной болезнью на разных участках нижних конечностей;
-
Оценить различия Р2-рецептор-опосредованных ответов большой подкожной вены у пациентов с варикозной болезнью в зависимости от степени венозной недостаточности и уровня венозного рефлюкса;
-
Изучить влияние антагонистов Р2-рецепторов - сурамина и PPADS - на сократительные ответы большой подкожной вены человека, вызванные электрической стимуляцией неадренергических, нехолинергических нервов;
-
Методами иммуногистохимии и иммунофлюоресценции оценить наличие и определить локализацию одтипов РХ- и Р2У-рецепторов ртерии желчного пузыря человека.
Научная новизна
В работе впервые установлено, что агонисты Р2-рецепторов - АТФ, ,-
метилен-АТФ и УТФ вызывают концентрационно-зависимые сокращения
изолированных артерии желчного пузыря, желудочно-сальниковой и лучевой
артерий человека, тогда как агонист Р2У-рецепторов 2-метилтио-АТФ приводит к
расслаблению ртерии желчного пузыря желудочно-сальниковой артерии
человека. Выявлены зличия кратительной тивности изолированных
5
проксимального и дистального участков варикозно-измененной большой подкожной
вены бедра человека в ответ на действие ,-метилен-АТФ, норэпинефрина и
гистамина. Установлена разница сократительного действия ,-метилен-АТФ на
изолированных дистальных и проксимальных участках большой подкожной вены
бедра, полученных от пациентов с варикозной болезнью с различной степенью
венозной недостаточности (хронических заболеваний вен) соответствии с
классификацией СЕАР. Показано отсутствие разницы во влиянии ,-метилен-АТФ на сократительную активность изолированной большой подкожной вены бедра, полученной от пациентов с различным уровнем ретроградного венозного рефлюкса вдоль ствола большой подкожной вены человека при варикозной болезни. Впервые описана рль Р-рецепторов осуществлении нйргенного онтроля онуа варикозно-измененной и здоровой большой пдкожной вены едр человека. Иммуногистохимическим и иммунофлюоресцентным методами исследования впервые выявлено наличие различных подтипов Р2-рецепторов в стенке артерии желчного пузыря человека и определена их локализация.
Научно-практическая значимость исследования
Результаты исследования углубляют и расширяют знания о наличии и функциональной активности Р-рецепторов рганиме еловека, дополняют знания о роли этих рецепторов в физиологических и патофизиологических условиях, подтверждают вероятное значение Р2-рецепторов кк потенциальных мишеней действия будущих лекарств. Данные об изменении функциональной активности Р2-рецепторов при варикозной болезни вен свидетельствуют о возможном участии этих рецепторов в патогенезе этого заболевания. Проведенное исследование открывает перспективы для поиска потенциальных вено-тонизирующих лекарственных средств среди агонистов Р2-рецепторов, которые могли бы использоваться при лечении варикозной болезни нижних конечностей.
Реализация результатов исследования
Результаты работы внедрены в лекционные курсы по фармакологии для
студентов лечебного, педиатрического и фармацевтического факультетов на кафедре
фармакологии и кафедре фармакологии фармацевтического факультета с курсами
фармакогнозии ботаники Казанского государственного медицинского
университета, а также в лекционный курс по хирургическим болезням для студентов
педиатрического и стоматологического факультетов и ординаторов на кафедре
хирургических лезней №2 Казанского сударственного едицинского
университета.
Положения, выносимые на защиту
-
Агонист Р2Х-рецепторов ,-метилен-АТФ вызывает концентрационно-зависимый сосудосуживающий эффект на изолированных артерии желчного пузыря, желудочно-сальниковой артерии и лучевой артерии человека, сила которого превышает вазоконстрикторное действие АТФ и УТФ на этих артериях. Агонист Р2У-рецепторов 2-метилтио-АТФ вызывает расслабление тонизированных артерии желчного пузыря и желудочно-сальниковой артерии.
-
Проксимальный и дистальный участки варикозно-измененной большой подкожной вены бедра человека проявляют разную чувствительность к агонисту Р2Х-рецепторов ,-метилен-АТФ, имея при этом одинаковую чувствительность к норэпинефрину и гистамину.
6 3. Р2Х1-, Р2Х2-, Р2Х3- и Р2У2-рецепторы представлены в гладкомышечном слое артерии желчного пузыря человека, 2Y і-рецепторы имеются ак а гладкомышечных, ак и на эндотелиальных летках, Р2У4-рецепторы представлены только на эндотелиальных клетках.
Степень достоверности и апробации работы
Высокая степень достоверности полученных результатов снована а
достаточном объеме экспериментальных данных, проведенных с использованием
современных методов исследования, адекватных поставленным задачам. Результаты
исследования, изложенные в диссертации, были доложены и обсуждены на 2-ом
съезде Российского научного общества фармакологов (Москва, 21-25 апреля 2003
г.), на 77, 78, 79, 80 и 81-ой Всероссийских студенческих научных конференциях
Казанского государственного медицинского университета, (Казань, 2003, 2004, 2005,
2006, 2007 г.), на XI-ом Рссийском национальном конгрессе «Человек и
лекарство» (Москва, 19-23 прля 2004 .), н международном импзиум
«Biological Motility» (Пущино, 23 мая - 1 июня 2004 г.), на конкурсе работ
участников «Открытого оссийского онкурса а лучшую научную аботу
студентов 2003 года» по разделу «Медицинские науки» (Москва, 2004 г.), на
Пироговской студенческой научной конференции Российского государственного
медицинского университета (Москва, 18 марта 2004 г.), на ХГХ-ом Съезде
физиологического общества им. И.П. Павлова, (Екатеринбург, 19-24 сентября 2004
г.), на V-ом Всероссийском съезде анатомов, гистологов и эмбриологов (Казань, 17-
18 сентября 2004 г.), на научно-практической конференции «Современные проблемы
экспериментальной и клинической медицины», (г. Паттайа, Таиланд, 15-25 января
2004 г.), на П-ой научно-практической конференции студентов и молодых ученых
«Медицина третьего тысячелетия глазами молодых» Марийского государственного
университета (Йошкар-Ола, 2005 г.), на 1-ой конференции «Качественное
использование карств фармаконадзор» международным частием,
приуроченной к 20-летию основания кафедры клинической фармакологии
фармакотерапии Казанской государственной медицинской академии (Казань, 12-14
октября 2005 г.), на 4-ой Международной конференции «Биологические основы
индивидуальной чувствительности к психотропным средствам» (Москва, 13-16
марта 2006 г.), на Российской конференции, посвященной 75-летию профессора И.А.
Студенцовой «Фармакология и токсикология фосфорорганических соединений и
других биологически активных веществ» (Казань, 25-26 ноября 2008 г.), на 13-ой
ежегодной сессии Научного центра сердечно-сосудистой хирургии им. А.Н.
Бакулева РАМН с Всероссийской конференцией молодых ученых (Москва. 17-19
мая 2009 г.), на XVI-ой Всероссийской аучно-практической конференции
«Молодые ученые в медицине» Казанского государственного медицинского
университета (Казань, 22-23 апреля 2011 г.), на Ш-ем Всероссийском научно-
практическом семинаре для олодых ученых «Методологические аспекты
экспериментальной клинической фармакологии» (Волгоград, 2011 г.), на
международном симпозиуме «UK Purine club 2011» (г. Кардифф, Великобритания, 2
ноября 2011 г.), на Китайско-Американско-Российском симпозиуме по клинической
и трансляционной медицине - «Кардиоваскулярные Цереброваскулярные
заболевания в фундаментальных и клинических трансляционных исследованиях и
клинической практике» (Харбин, 27-29 июля 2012 .) а IV-ом ъезде
7 фармакологов России «Инновации в современной фармакологии» (Казань, 18-21 сентября 2012 г.).
Публикации
По теме диссертации опубликовано 34 печатные работы, в том числе, 7 статей в ведущих рецензируемых научных журналах, рекомендованных ВАК Минобрнауки РФ для публикации результатов диссертационных исследований.
Объем и структура диссертации
Нейрональный контроль тонуса большой подкожной вены бедра человека
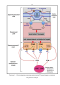
Такое совместное действие норэпинефрина и АТФ обеспечивает быструю вазоконстрикцию в ответ на симпатический стимул (Рисунок 1), поскольку АТФ активирует быстрые ионные каналы Р2Х-рецепторов, которые в ответ пропускают ионы кальция, вызывают деполяризацию мембраны, и активацию потенциал-зависимых кальциевых каналов [71]. Одновременно, норэпинефрин активирует 17 адренорецепторы с последующей вазоконстрикцией, но данный эффект развивается существенно медленнее, поскольку эффект норэпинефрина опосредован через систему G-белка. В результате, содружественное выделение АТФ и норэпинефрина вызывает две различные фазы деполяризации гладкомышечных клеток: 1) быструю деполяризацию (или возбуждающий постсинаптический потенциал), которая полностью угнетается антагонистами Р2Х-рецепторов; 2) медленную деполяризацию, которая ингибируется альфа адреноблокаторами [135, 24, 119]. Такое синергичное действие норэпинефрина и АТФ характерно для большинства исследованных артерий [41], хотя существуют примеры полного отсутствия пуринергического компонента симпатической иннервации, например в подкожных и желудочно-сальниковых артериях человека [105, 70]. Исследования показали, что количество Р2Х1 -рецепторов выше в мышечных артериях среднего калибра, по сравнению с более крупными эластичными артериями [95], что возможно объясняется более плотной иннервацией мышечных сосудов среднего калибра, по сравнению с крупными сосудами [33]. Помимо Р2Х1 -рецепторов аналогичное вазоконстрикторное действие возникает при стимуляции Р2Х2- и Р2Х4-рецепторов [40, 41]. Кроме прямого действия на гладкомышечные клетки, выделяемая из нервных терминалей АТФ также действует на Р2Y-рецепторы расположенные на самом нервном окончании, обеспечивая тем самым контроль за высвобождением медиаторов по принципу отрицательной обратной связи (Рисунок 1) [73, 27]. При этом, продукт распада АТФ - аденозин - активирует пресинаптические аденозиновые А1 рецепторы, которые действуют синергично Р2Y-рецепторам и ингибируют процесс высвобождения медиаторов [29, 81] (за исключением почечных сосудов, в которых А1 рецепторы отсутствуют на поверхности симпатических нервов [130]).
Таким образом, роль АТФ в качестве медиатора очень важна для поддержания тонуса кровеносных сосудов, поскольку АТФ обеспечивает быстроту ответа на нервный стимул и контроль за количеством высвобождаемого медиатора. Роль АТФ в качестве эндотелий-зависимого вазодилататора
Кроме нервных окончаний, значительная часть внеклеточно-активной АТФ содержится в эндотелиальных клетках кровеносных сосудов [41, 118]. Одной из важнейших функций эндотелиальных клеток является обеспечение вазодилатации, тем самым противодействуя и уравновешивая действие норэпинефрина и АТФ, выделяющихся из симпатических нервных окончаний и опосредующих вазоконстрикцию.
В условиях гипоксии или резкого повышения скорости кровотока {shear stress) АТФ выделяется из эндотелиальных клеток в просвет кровеносного сосуда. Путем паракринной и аутокринной стимуляции, АТФ активирует преимущественно P2Yb P2Y2 и Р2Х4 подтипы рецепторов (Рисунок 1) [41, 118] . В ответ на данный стимул, эндотелиальные клетки выделяют три основных вазорелаксанта - оксид азота (N0), эндотелиальный фактор гиперполяризации и простациклин, вызывая тем самым расслабления тонуса сосудистой стенки [28, 125]. P2Yi подтип рецепторов наиболее часто представлен на поверхности эндотелия кровеносных сосудов и активируется аденозиндифосфатном (АДФ) [120], образующимся в процессе энзиматического распада АТФ. Уридинтрифосфорная кислота (УТФ) является еще одним нуклеотидом, способным активировать некоторые подтипы Р2-рецепторов, который также выделяется в кровоток из эндотелиальных клеток в условиях гипоксии или резкого повышения тонуса [158]. АТФ и УТФ в равной степени способны активировать эндотелиальный P2Y2 подтип рецепторов, вызывая вазодилатацию [88].
Интересным фактом является то, что активация Р2Х4 подтипа рецепторов, расположенных на эндотелиальных клетках, также приводит к расслаблению сосудистой стенки, эффект, который присущ в основном Р2У-рецепторам. Установлено, что эндотелий-опосредованная дилятация в ответ на изменение гемодинамики {shear stress) была значительно менее выражена у мышей, нокаутных по гену Р2Х4-рецептора; у таких мышей было также повышено артериальное давление и существенно снижена продукция оксида азота (N0) [82]. У людей с мутацией в гене Р2Х4-рецептора (со значительным снижением функции этого ионного канала) наблюдалось повышенное пульсовое давление, что возможно связанно с нарушением эндотелий-зависимой функции вазодилатации, опосредованной Р2Х4-рецептором [14]. Другие подтипы Р2-рецепторов (P2Y4, P2Y6, Р2Уц, Р2Х1 и Р2Х6) также были найдены на эндотелиальных клетках, однако их влияние на тонус кровеносных сосудов существенно менее значимое, а иногда и противоречивое [119, 41, 118]. Любопытно, что эндотелиальные Р2Х1-рецепторы, которые принято считать чисто вазоконстрикторными, в брыжеечных сосудах крысы вызывают эндотелий-зависимое расслабление, которое не ингибируется блокатором NO-синтетазы [74]. Это свидетельствует о том, что эндотелиальные Р2Х1 рецепторы активирует иной механизм вазорелаксации, не зависящий от продукции оксида азота (N0).
В дополнении к Р2-рецептор-опосредованному расслаблению сосудов, активация эндотелиальных и гладкомышечных аденозиновых А2 рецепторов (подтипы А2А и А2В) также приводит к снижению тонуса кровеносных сосудов [146].
Важность эндотелия в целом, и эндотелиальных Р2-рецепторов в частности, в процессе расслабления сосудистой стенки очевидна на примере повреждения эндотелиального слоя сосуда. В результате такого повреждения происходит активация тромбоцитов и лейкоцитов, которые устремляются к месту повреждения и прикрепляются к поврежденной стенке сосуда. В активированном состоянии и тромбоциты и лейкоциты выделяют АТФ, АДФ и УТФ. В норме эти нуклеотиды взаимодействовали бы с Р2-рецепторами на поверхности эндотелиальных клеток и вызывали вазодилятацию. Однако, в условиях повреждения эндотелиального слоя, происходит активация Р2-рецепторов, расположенных на гладкомышечных клетках, что приводит в сокращению сосуда и возникает локальных вазоспазм [41, 118].
Исследование механической активности изолированных кровеносных сосудов человека
Артерия желчного пузыря человека была исследована на наличие и локализацию различных подтипов Р2-рецепторов иммунофлюоресцентным и иммуногистохимическим методами.
Для проведения этих экспериментов от пациентов были получены сегменты сосудов длинной 1-2 см. Сосуды моментально помещали в охлажденный физиологический раствор Кребса (4С, рН = 7.3-7.4) и транспортировали в лабораторию. В лаборатории кровеносные сосуд отделяли от окружающей ткани и фиксировали в течение 4 часов в 4% растворе формальдегида. После фиксации сегменты сосудов помещали в Tissueek Optimum Cutting Temperature Compound (Sakura Finetek) и в таком виде замораживали в изопентане, охлажденном в жидком азоте. Такая методика обеспечивала быструю и равномерную заморозку ткани. Замороженные сегменты сосудов нарезали при помощи креостата (Reichert Jung СМ1800, Leica Instruments, Нуслох, Германия), толщина срезов составляла 12 м. Креостатные срезы сосудов сразу же помещались на желатинизированные предметные стекла. Предметные стекла с образцами ткани хранили в морозильной камере до начала эксперимента (но не более 7 суток). Методика иммунофлюоресцентного окрашивания сосудов
Для иммунофлюоресцентного окрашивания использовали методику описанную ранее [47]. Готовые к эксперименту предметные стекла со срезами кровеносных сосудов промывали физиологическим раствором, забуференным фосфатным буфером (далее PBS) при комнатной температуре 3 раза по 5 минут каждый раз удаляя старый и добавляя новый раствор PBS. Далее, с целью предотвращения неспецифического окрашивания, предметные стекла с тканью помещались во влажную камеру и срезы обрабатывали и инкубировали в течение 20 минут в 10% растворе нормальной неиммунной сыворотки лошади, разведенной в PBS, содержащем 0.05% мертиолата (merthiolate/thimerosal - Sigma Catalogue # T-5125).
Затем срезы кровеносных сосудов инкубировали в первичных Р2-рецептор-специфичных поликлональных кроличьих антителах. Все антитела разводились в 10% растворе нормальной неиммунной сыворотки лошади, разведенной в PBS, содержащем 0.05% мертиолата, в соотношении 1:200 (антитело : растворитель). Данная инкубация проводилась в течение 14-16 часов (обычно ткань оставляли инкубироваться на ночь) при комнатной температуре во влажной камере. За время данной инкубации первичные антитела связывались с соответствующим рецептором в стенке кровеносного сосуда.
После завершения этапа инкубации с первичными антителами, предметные стекла со срезами ткани промывали в PBS (как описано выше) для удаления несвязанных с тканью первичных антител. Все последующие стадии проводились со светочувствительными реагентами, поэтому они выполнялись в темноте или при минимальном освещении. После промывки стекла с тканью помещали во влажную камеру для инкубации со вторичными антителами типа Oregon Green (goat anti-rabbit IgG), конъюгированными с флюорохромами. Вторичные антитела также разводились в PBS, содержащем 0.05% мертиолата, но в соотношении 1:100 (антитело : растворитель). Разведенные вторичные антитела наносились на срезы с тканью и инкубировались в течение одного часа при комнатной температуре. На данной стадии эксперимента вторичные антитела специфически связывались с первичными антителами, которые в свою очередь связаны с Р2-рецепторами в стенке сосудов. После завершении инкубации со вторичными антителами, предметные стекла со срезами ткани ещё раз промывали в PBS для удаления несвязанных с тканью вторичных антител. Не позволяя ткани высохнуть на нее наносился раствор Citifluor (Citifluor Ltd, Лондон, Великобритания), содержащий глицерин и PBS. Поверх этого раствора накладывалось покровное стекло. Схематично методика проведения иммунофлюоресцентного окрашивания сосудов представлена на Рисунке 10.
Методика иммуногистохимического окрашивания сосудов Для иммунофлюоресцентного окрашивания использовали методику описанную ранее [156, 96]. После промывки предметных стекол по методике, описанной выше, образцы ткани обрабатывали 50% раствором метанола, содержащего 0.4% пероксида водорода (Н2О2), в течение 10 минут с целью блокировки активности эндогенной пероксидазы. По аналогии с методикой иммунофлюоресцентного окрашивания, неспецифическое окрашивание блокировали инкубацией ткани в 10% растворе нормальной неиммунной сыворотки лошади (разведенной в PBS, содержащем 0.05% мертиолата) на протяжении 20 минут. Дальнейший этап обработки ткани первичными антителами был полностью идентичен аналогичному этапу методики иммунофлюоресцентного окрашивания (описано выше). Все этапы обработки ткани проводились при комнатной температуре. После инкубации с первичными антителами, предметные стекла со срезами сосудов обрабатывали вторичными антителами биотинилированными антителами (donkey anti-rabbit immunoglobulin G) в разведении 1:500 в 1% растворе нормальной неимунной сыворотки лошади в Воздействие ультрафиолетовыми лучами вызывает свечение
PBS, содержащем 0.05% мертиолата. Время инкубации со вторичными антителами составляло 1 час. Затем, ткань в течение 30 минут обрабатывали ExtrAvidin-пероксидазой хрена, разведенной в соотношении 1:1000 в растворе PBS, содержащем 0.05% мертиолата. На последнем этапе для окрашивания участков ткани, с которыми связались первичные антитела, ткань инкубировали с раствором, содержащим: 0.05% 3,3 -диаминобензидин (субстрат для пероксидазы хрена), 0.04% сульфат никеля(П)-аммония, 0.1 М фосфат натрия, 0.004% хлорид аммония, 0.2% глюкозы, 0.1% глюкозооксидазы. Данную реакцию проводили в течение 5 минут, после чего ткань отмывали, дегидратировали при помощи изопропилового спирта, покрывали фиксирующей средой Eukitt (BDH, Пул, Великобритания) и накрывали покровным стеклом. В таком виде препараты сосудов были готовы для микроскопирования.
Влияние норэпинефрина, гистамина и агонистов Р2-рецепторов на механическую активность лучевой артерии
Сравнение влияния агониста Р2-рецепторов а,Р-метилен-АТФ и антагониста Р2-рецепторов PPADS на варикозно-измененной и не пораженной варикозной болезнью большой подкожной вене человека а,Р-метилен-АТФ (0.1-30 fiM) вызывал концентрационно-зависимые сокращения большой подкожной вены, полученной как от пациентов с варикозной болезнью, так и от пациентов без варикозной болезни (Рисунки 33 и 34). Величина pD2 (отрицательный логарифм ЕС5о) для а,3-метилен-АТФ, рассчитанная для пациентов с варикозной болезнью и без нее составила 5.72 ± 0.06 (п=7) и 6.16 ± 0.09 (п=6), что статистически достоверно отличается друг от друга (р 0.05).
Интересно, что инкубация большой подкожной вены пациентов с варикозной болезнью с PPADS в концентрации 10 fiM никак не изменяла сократительного ответа вены в ответ на а,3-метилен-АТФ и графики «концентрация-эффект» для этого агониста до и после инкубации с PPADS практически совпадали (Рисунок 33). lg [а.р-метилен-АТФ, М] Рисунок 33 - Сокращения изолированной большой подкожной вены пациентов варикозной болезнью вен, вызванные а,3-метилен-АТФ до (светлые символы) и после (темные символы) инкубации с PPADS в концентрации 10 fiM. Результаты представлены в виде М ± m (п=6-7) По-другому реагировала большая подкожная вена пациентов без варикозной болезни - график "концентрация-эффект" для а,3-метилен-АТФ после инкубации с 10 fiM PPADS заметно отклонялся книзу, что свидетельствует об антагонистическом действии вещества. Однако, проведенный статистический анализ с использованием t критерия Стьюдента для связанных величин выявил достоверную разницу в ответах большой подкожной вены на а,3-метилен-АТФ до и после PPADS лишь в двух наивысших концентрациях агониста (Рисунок 34). 401 Є До инкубации с PPADS S Е После инкубации с 10 цМ PPADS 30 га сокращенияо о Б О -8 -7 -6 -5 і-4 lg [а,р-метилен-АТФ, М] Рисунок 34 - Сокращения изолированной большой подкожной вены пациентов с облитерирующим атеросклерозом, вызванные а,3-метилен-АТФ до (светлые символы) и после инкубации с PPADS в концентрации 10 fiM (темные символы). Результаты представлены в виде М ± m (п=6-7). - р 0.05 3.6. Зависимость сократительной способности варикозно-измененной большой подкожной вены от протяженности рефлюкса и класса хронических заболеваний вен
Для определения зависимости сократительной способности большой подкожной вены от протяженности рефлюкса всем пациентам было выполнено ультразвуковое дуплексное сканирование большой подкожной вены (GE Vivid 3). Пациенты с варикозной беленью были разделены на 2 группы: первая группа -пациенты с рефлюксом по большой подкожной вене до верхней трети голени (10 человек), вторая группа - пациенты с тотальным рефлюксом по большой подкожной вене (12 человек).
При определении зависимости сократительной активности большой подкожной вены от выраженности патологических изменений (клинических, этиологических, анатомических и патофизиологических) в венозной системе нижних конечностей использовали классификацию СЕАР [127]. Пациенты были также разделены на 2 группы: первая группа - пациенты с классами С2-3, вторая группа - С4-6.
При разделении пациентов по группам в зависимости от класса хронического заболевания вен было выявлено, что в проксимальном участке большой подкожной вены сократительная способность на норэпинефрин существенно выше у пациентов с С2-3, чем у пациентов с С4-6 (Рисунок 35), что статистически подтверждается значениями pD2: 6.21 ± 0.19 (п=14) для большой подкожной вены, полученных от пациентов с классом С2-3 и 5.44 ± 0.13 (п=8) для большой подкожной вены, полученных от пациентов с классом С4-6 (р 0.01). Однако при проведении аналогичного сравнения для дистального участка большой подкожной вены, разницы между сократительными ответами вен, полученных от пациентов с С2-3 и С4-6 классов, в ответ на норэпинефрин выявлено не было, величина pD2 соответственно составила 6.15 ± 0.11 (п=14) и 6.18 ± 0.08 (п=8) (р 0.05) (Рисунок 36). о .,„ 2 150- ш Е 3 CN га ЮО- X к 5 X ф 3 га БО- СІ. О о н j/" / -- о 3« о- -7.0 -6.5 -6.0 -5.5 -5.0 -4.5 lg [норэпинефрин, M] Рисунок 35 - Сокращения изолированного проксимального участка варикозно измененной большой подкожной вены бедра человека, вызванные норэпинефрином. Белые квадратики - участки БПВ, полученные от пациентов с классом С2-3. Черные квадратики - участки БПВ, полученные от пациентов с классом С4-6. Результаты представлены в виде М ± m (п=8-14). - р 0.05 Рисунок 36 - Сокращения изолированного дистального участка варикозно измененной большой подкожной вены бедра человека, вызванные норэпинефрином. Белые квадратики - участки БПВ, полученные от пациентов с классом С2-3. Черные квадратики - участки БПВ, полученные от пациентов с классом С4-6. Результаты представлены в виде М ± m (п=8-14) Иная картина была получена при сравнении сократительной активности вен от пациентов с разными классами хронических заболеваний вен в ответ на метил ен-АТФ. Проксимальный участок большой подкожной вены имел схожую реакцию на ,-метилен-АТФ с реакцией на норэпинефрин и в трех наивысших концентрациях (3, 10 и 30 fiМ) сократительная способность вен от пациентов с меньшим классом хронических заболеваний вен была достоверно выше таковой участков вен, полученных от пациентов с большим классом хронических заболеваний вен (Рисунок 37). При этом, величина pD2 для ,-метилен-АТФ на проксимальных участках вен пациентов с С2-3 составила 6.12 ± 0.18 (п=14), а для пациентов с С4-6 - 5.87 ± 0.19 (п=8), что не достигало уровня статистической достоверности.
Дистальные участки вен проявляли схожую сократительную реакцию на ,-метилен-АТФ с проксимальными участками большой подкожной вены и с увеличением класса хронических заболеваний вен кривая «концентрация-эффект» смещалась вправо (Рисунок 38). Значение pD2 для вен С2-3 в ответ на ,-метилен-АТФ составило 4.89±0.09 (п=14), а для вен С4-6 составило 5.57 ± 0.09 (п=8) (р 0.001).
При разделении пациентов по группам в зависимости от протяженности рефлюкса крови по стволу большой подкожной вены статистически значимых отличий между двумя группами выявлено не было. В проксимальных участках большой подкожной вены ни в ответ на норэпинефрин (Рисунок 39), ни в ответ ,-метилен-АТФ (Рисунок 40) не удалось выявить статистических различий максимальных сокращений и значений pD2 между группами пациентов с уровнем рефлюкса до верхней трети голени и тотальным рефлюксом по всей длине большой подкожной вены. Аналогичная картина была выявлена и на дистальных участках большой подкожной вены.
Зависимость сократительной способности варикозно-измененной большой подкожной вены от протяженности рефлюкса и класса хронических заболеваний вен
Наличие и активность Р2-рецепторов в варикозных и неварикозных больших подкожных венах человека были показаны ранее в нашей [8, 161, 2] и других лабораториях [21]. Нами были обнаружены различные подтипы Р2-рецепторов в гладкомышечных тканях и эндотелиальном слое большой подкожной вены [5]. В то же время, степень вовлечения этих рецепторов в формировании тонуса большой подкожной вены оставалась не изученной. Результаты настоящего исследования подтверждают, что Р2-рецепторы являются важной частью системы нейрогенного контроля тонуса этого кровеносного сосуда, как в норме, так и при патологии. Также, выявленный неадренергический и нехолинергический компонент нервной передачи свидетельствует о наличии эндогенных лигандов (таких как АТФ), выделяющихся при стимуляции нервов и действующих посредством Р2-рецепторов. В предыдущих исследованиях на различных кровеносных сосудах человека и животных было показано, что АТФ выделяется из нервных окончаний нервов (симпатических и сенсо-моторных) совместно с другими нейромедиаторами, действуя в качестве ко-трансмиттера [35, 41]. Действуя содружественно с норэпинефрином (при совместном экзоцитозе из симпатических нервов), в кровеносных сосудах АТФ чаще всего действует на Р2Х1 подтип рецепторов и также вызывает сокращение гладкомышечных клеток. При выделении из окончаний сенсо-моторных нейронов, АТФ чаще всего действует на Р2Y1 2,6 или Р2Y12 подтип рецепторов вызывая либо сокращение, либо расслабление сосуда [41].
Р2-рецепторы в БПВ могут играть сразу несколько важных ролей. Существует теория, что Р2-рецепторная система эволюционно гораздо более ранняя, нежели другие рецепторные системы [32]. В связи с этим, можно предположить, что в кровеносных сосудах человека Р2-рецепторная система уступает первенство в реализации вазомоторного эффекта более эволюционно-развитым системам, например, адренергической. В то же время, роль Р2-рецепторов существенно возрастает при возникновении патологических состояний, таких как воспаление, боль, тромбоз и вазоспазм [36, 3]. Таким образом, можно предположить, что Р2-рецепторы это своеобразный защитный механизм, который организм человека может активировать при развитии патологического процесса. В частности, при варикозной болезни имеет место перестройка Р2-рецепторного аппарата в БПВ, которая проявляется в изменении чувствительности Р2-рецепторов к действию агонистов и антагонистов на различных участках большой подкожной вены [9]. Такая перестройка может свидетельствовать о вовлеченности Р2-рецепторов в патогенез развития варикозной болезни, который на сегодняшний день остается не до конца изученным. Результаты настоящего исследования показали, что эффективность адрено, холино- и Р2-рецепторов меньше в варикозно-измененных венах по сравнению с венами без варикозного повреждения. Это позволяет предположить, что в процессе развития варикозной болезни происходит перестройка не только адрено- и холинорецепторов, но и Р2-рецепторов тоже. Однонаправленное вовлечение всех исследованных нами рецепторных систем в сторону понижения их эффективности может свидетельствовать о генерализованой потере рецептор-опосредованных ответов в варикозных венах, что может объясняться перестройкой большой подкожной вены сократительного типа в вену синтетического типа [164]. Конечно, интерпретацию этих данных и сравнение варикозных и не-варикозных вен следует проводить с осторожностью, поскольку исследования проводились на участках БПВ разной локализации.
В данном исследовании мы подтвердили свой ранее сделанный вывод о том, что варикозная болезнь существенно нарушает Р2-рецептор-опосредуемые ответы [8]. Мы установили, что величина pD2, вычисленная для ,-метилен-ATФ в опытах на большой подкожной вене пациентов с варикозной болезнью, было достоверно меньше по сравнению с таковой, найденной на большой подкожной вене пациентов, не страдающих этой болезнью. Различия в ответах большой подкожной вены пациентов с варикозной болезнью и без этого заболевания вероятно связаны в основном с уменьшением числа чувствительных к ,-метилен-ATФ рецепторов семейства Р2Х при варикозной болезни. Вместе с тем, возможно при этом заболевании происходит некоторая перестройка Р2 рецепторного аппарата, например, появление (или увеличение числа) Р2Х4 рецепторов, которые нечувствительны к действию PPADS [106]. Другим объяснением отсутствия эффекта PPADS на большой подкожной вене при варикозной болезни может быть появление аллостерических регуляторных участков Р2Х-рецепторов, изменяющих их чувствительность к действию агонистов и антагонистов.
К настоящему времени более двух десятков соединений описаны как антагонисты Р2-рецепторов, однако следует признать, что ни одно из них не обладает достаточной селективностью к подтипам Р2-рецепторов [89]. Одним из наиболее широко используемых соединений в качестве Р2 антагониста является PPADS. Было показано, что PPADS проявляет выраженное антагонистическое действие по отношению к периферическим Р2Х-рецепторам, не влияя на эффекты, опосредуемые - М-холино-, альфа-адрено- и гистаминорецепторами [134, 4]. Хотя в последующем был выявлен определенный антагонизм PPADS и к Р2У-рецепторам [59], в фармакологических экспериментах на изолированных тканях соединение относительную селективность по отношению к Р2Х-рецепторам в концентрациях не выше 10 fiМ [89, 106].
В наших экспериментах на изолированных сосудах человека PPADS проявил разную эффективность - в одной и той же концентрации он практически полностью угнетал сократительные ответы артерии желчного пузыря на ,-метилен-АТФ, не изменял сократительные ответы большой подкожной вены пациентов с варикозной болезнью вен и в небольшой степени снижал ответы большой подкожной вены пациентов, не страдающих варикозом. Возможно это связано с тем, что, как мы установили в этой работе, в артерии желчного пузыря человека имеется большое представительство Р2Х1 или Р2ХЗ рецепторов, а ,-метилен-АТФ является селективным агонистом именно этих подтипов Р2-рецепторов, и именно они наиболее чувствительны к действию PPADS [106].
Симпатическая ко-трансмиссия норэпинефрина, АТФ и нейропептида Y была установлена и в большой подкожной вене бедра человека [17, 97]. Фармакологические эксперименты показали концентрационно-зависимые ответы большой подкожной вены на АТФ, УТФ и ,-метилен-АТФ, которые были существенно более выраженные в здоровых венах, по сравнению с венами, пораженными варикозной болезнью [8, 161]. Возможно, что обнаруженное снижение Р2Х1-рецептор-опосредованных сокращений и повышение экспрессии Р2Yi и Р2Y2 подтипов рецепторов при варикозной болезни является частью патогенеза развития данного заболевания [21]. Таким образом, в данной работе нами получены новые сведения о различной эффективности Р2Х агониста ,-метилен-АТФ и Р2 антагониста PPADS на артериях и венах человека. Эти результаты позволяют предположить вероятное вовлечение Р2-рецепторов в регуляцию сосудистого тонуса и локального кровообращения в организме человека. Проведенное нами исследование свидетельствует о наличии неадренергического и нехолинергического компонента нервной передачи в большой подкожной вене. Эффективность антагонистов Р2 -рецепторов - PPADS и сурамина, позволяет предположить, что частью неадренергического и нехолинергического компонента нервной регуляции тонуса большой подкожной вены является Р2-рецептор опосредованный компонент. Дальнейшее детальное изучение роли Р2-рецепторов в большой подкожной вене позволит уточнить их роль в патогенезе развития различных заболеваний венозной системы человека (таких как варикозная болезнь, тромбофлебит, и т.д.), а также создает предпосылки для создания лекарственных средств, которые бы действовали посредством активации или ингибирования Р2-рецепторов.